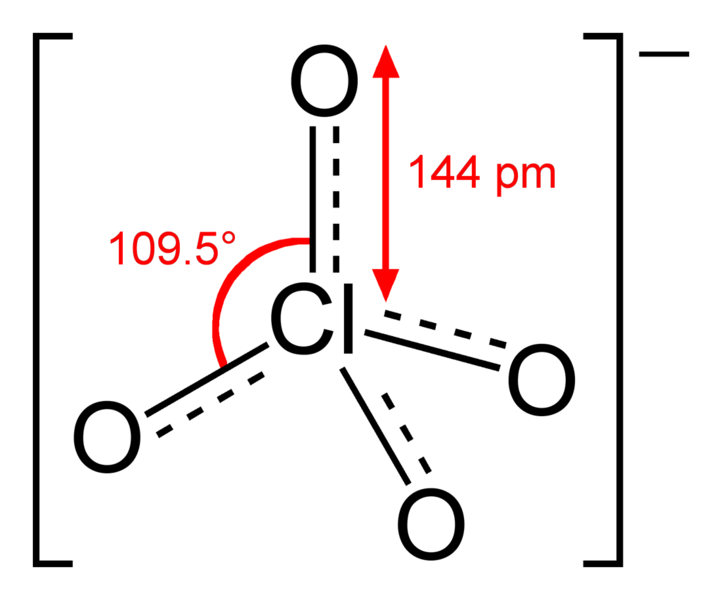
Magnesiumperchlorat ist das Magnesiumsalz der Perchlorsäure HClO4. Es ist ein chemischer Feststoff mit der Formel Mg(ClO4)2.
Eigenschaften
Magnesiumperchlorat ist ein starkes Oxidationsmittel und gibt beim Erhitzen Sauerstoff ab. Deshalb ist es stark brandfördernd. Mit brennbaren Verbindungen bildet Magnesiumperchlorat explosive Mischungen, die schlagempfindlich sind und gegebenenfalls bereits beim Vermengen detonieren. Die Herstellung solcher Mischungen verbietet sich daher von selbst. Magnesiumperchlorat, das mehr als 2 % brennbare Verunreinigungen enthält, fällt unter das Sprengstoffgesetz.
Magnesiumperchlorat ist äußerst hygroskopisch. Der Wasserdampf-Partialdruck über wasserfreiem Magnesiumperchlorat (sogenanntes Anhydron) beträgt lediglich 70 mPa, der über dem Dihydrat (Mg(ClO4)2·2H2O, Dehydrit) 300 mPa bei 20 °C (zum Vergleich: 3 mPa über Phosphor(V)-oxid). Es wird daher als Trockenmittel für nicht oxidierbare Stoffe verwendet, da es zudem auch eine hohe Trockenkapazität besitzt. Die Wasserabsorption ist ein sehr exothermer Prozess.
Magnesiumperchlorat ist in Wasser und polaren organischen Lösungsmitteln gut löslich.
Einzelnachweise